cần lấy bao nhiêu lít khí hidro và nito để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí dều được đo trong cùng một điều kiện nhiệt độ , áp suất hiệu suất của phản ứng là 25%.

Những câu hỏi liên quan
cần lấy bao nhiêu lít khí hidro và nito để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí đều được đo trong cùng một điều kiện nhiệt độ , áp suất hiệu suất của phản ứng là 25%.
Khi hiệu suất đạt 25% thì được 67.2 lít
Theo lí thuyết sẽ là 100% hay khi đó =67,2 x 4=268.8 lit =12mol
N2 +3H2 =>2NH3
6<.......18<.......12
vN2 =6 x 22,4 =134.4lit
vH2 =1 x 22,4=403,2LIT
Đúng 0
Bình luận (0)
cần lấy bao nhiêu lít khí hidro và nito để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí đều được đo trong cùng một điều kiện nhiệt độ , áp suất hiệu suất của phản ứng là 25%.
cần lấy bao nhiêu lít khí hidro và nito để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí đều được đo trong cùng một điều kiện nhiệt độ , áp suất hiệu suất của phản ứng là 25%.
N2 + 3H2 => 2NH3
33,6 100,8 <= 67,2
mà H= 25%
=> VN2 = 134,4
VH2= 403,2
Đúng 0
Bình luận (0)
Cần lấy bao nhiêu lít khí
N
2
và
H
2
để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%. A. 33,6 lít
N
2
và 100,8 lít
H
2
.
B. 8,4 lít
N...
Đọc tiếp
Cần lấy bao nhiêu lít khí N 2 và H 2 để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%.
A. 33,6 lít N 2 và 100,8 lít H 2 .
B. 8,4 lít N 2 và 25,2 lít H 2 .
C. 268,8 lít N 2 và 806,4 lít H 2 .
D. 134,4 lít N 2 và 403,2 lít H 2 .
Chọn D
Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
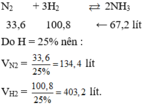
Đúng 0
Bình luận (0)
Cần bao nhiêu lít khí nitơ và khí hiđro để điều chế được 67,2 lit khí amoniac? Biết rằng thể tích của các khí đề được đo ở cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%?
Ta thấy tỉ lệ về thể tích cùng là tỉ lệ về số mol:
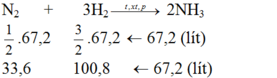
Tỉ lệ số mol cũng chính là tỉ lệ thể tích
Theo pt:
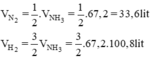
Do hiệu suất của phản ứng là 25% nên thể tích của nitơ và hiđro cần lấy là:
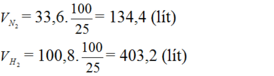
Đúng 0
Bình luận (0)
Cần lấy bao nhiêu lít khí nitơ và khí hiđro để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí đều được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%.
Với hiệu suất 25%, thể tích khí nitơ ở đktc là 134,4 lít; thể tích khí hiđro là 403,2 lít.
Đúng 0
Bình luận (0)
phải dùng bao nhiêu lít khí nito và bao nhiêu lít khí hidro để điều chế 17g NH3 . biết rằng hiệu suất chuyển hóa thành amoniac là 25% . Các thể tích khí được đo ở đktc .
N2 + 3H2 --> 2NH3
Số mol của NH3 là: nNH3(thực tế)= 17/17=1 (mol)
---> nN2 =1/2 nNH3 = 0.5 mol, nH2=3/2 nNH3=1.5 mol
Do thực tế NH3 sinh ra chỉ bằng 25% lượng NH3 có thể sinh ra. Vậy ta có:
nNH3 (100%) được sinh ra=nNH3(thực tế)*4=1*4=4mol
--> nN2( thực)= 0.5*4=2mol--> V N2 = 44,8 lít
nH2 (thực)=1,5*4 mol=6mol ---> VH2 = 134,4 lít
Số mol của NH3 là: nNH3(thực tế)= 17/17=1 (mol)
---> nN2 =1/2 nNH3 = 0.5 mol, nH2=3/2 nNH3=1.5 mol
Do thực tế NH3 sinh ra chỉ bằng 25% lượng NH3 có thể sinh ra. Vậy ta có:
nNH3 (100%) được sinh ra=nNH3(thực tế)*4=1*4=4mol
--> nN2( thực)= 0.5*4=2mol--> V N2 = 44,8 lít
nH2 (thực)=1,5*4 mol=6mol ---> VH2 = 134,4 lít
Đúng 0
Bình luận (0)
có pt: N2 + 3H2 = 2NH3
theo đề bài thì nNH3 =17/17=1 mol
suy ra từ phương trình thì nN2=1/2nNH3 *100/25=2 mol
vậy V N2=2*22,4=44,8 lit
va nH2=3/2 nNH3* 100/25 =6 mol
vậy V H2 =6*22,4= 134,4 lit
Đúng 0
Bình luận (3)
N2 + 3H2 --> 2NH3
Số mol của NH3 là: nNH3(thực tế)= 17/17=1 (mol)
---> nN2 =1/2 nNH3 = 0.5 mol, nH2=3/2 nNH3=1.5 mol
Do thực tế NH3 sinh ra chỉ bằng 25% lượng NH3 có thể sinh ra. Vậy ta có:
nNH3 (100%) được sinh ra=nNH3(thực tế)*4=1*4=4mol
--> nN2( thực)= 0.5*4=2mol--> V N2 = 44,8 lít
Đúng 0
Bình luận (0)
phải dùng bao nhiêu lít khí nito và bao nhiêu lít khí hidro để điều chế 17g NH3 . biết rằng hiệu suất chuyển hóa thành amoniac là 25% . Các thể tích khí được đo ở đktc .
. 44,8 lít N2 và 134,4 lít H2
Do hiệu suất 25 % nên thể tích N2, H2 cần gấp 4 lần so với lí thuyết.
Đúng 0
Bình luận (2)
phải dùng bao nhiêu lít khí nito và bao nhiêu lít khí hidro để điều chế 17g NH3 . biết rằng hiệu suất chuyển hóa thành amoniac là 25% . Các thể tích khí được đo ở đktc .










